
La Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) suspendió de forma preventiva las actividades de un laboratorio y prohibió el uso, comercialización y distribución de varios lotes de un medicamento para la prevención de las recidivas de colitis ulcerosa.
La medida fue oficializada mediante la Disposición 7254/2025, tras detectarse múltiples irregularidades en la fabricación del fármaco. El producto presentó deficiencias graves tanto en la materia prima como en el medicamento terminado.
¿Cuál es el medicamento prohibido por la ANMAT?
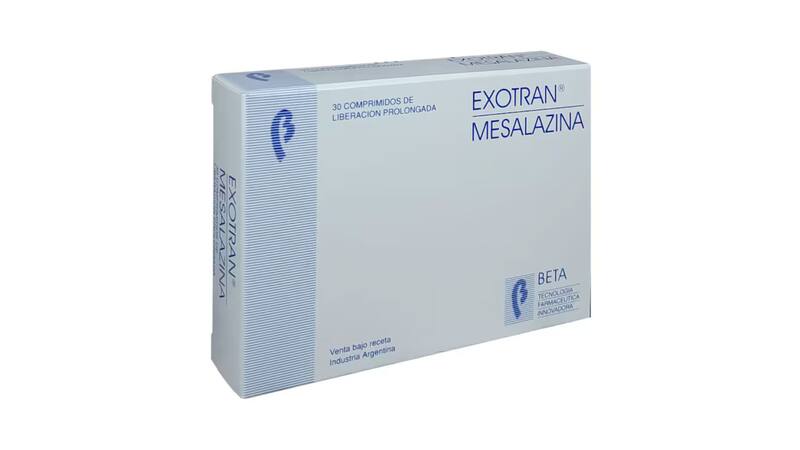
El fármaco afectado es Exotran, certificado REM N° 53.080, fabricado por Laboratorios Beta S.A. (CUIT N° 30-50152188-0). Se trata de un antiinflamatorio indicado para el tratamiento de la fase aguda y para la prevención de las recidivas de colitis ulcerosa, enfermedad de Crohn, protosigmoiditis, rectocolitis hemorrágica y proctitis.
Los lotes prohibidos son: 65.427, 65.752, 66.087, 66.445, 66.725, 67.002, 67.137, 67.504, 67.727 y 67.850, con vencimientos entre julio de 2025 y mayo de 2027.

La investigación comenzó tras la notificación de falta de efectividad en el lote 66.087. Los análisis oficiales confirmaron que el producto no cumplía con las especificaciones de calidad, especialmente en el ensayo de disolución, lo que explicaría su ineficacia.
Cuáles fueron las irregularidades detectadas
La ANMAT identificó deficiencias críticas y mayores en el sistema de calidad farmacéutico, producción y control de calidad del laboratorio. Entre los hallazgos más graves se destacan:
- Proveedor de Mesalazina no calificado correctamente: sin archivo maestro de la droga ni certificaciones GMP/ISO válidas.
- Problemas en la materia prima: conservación deficiente, trazabilidad inconsistente, ausencia de ensayos de impurezas genotóxicas y nitrosaminas.
- Producto terminado con fallas: muestras fuera de especificación, ensayos faltantes (impurezas, humedad, dureza), resultados erróneos y estudios de estabilidad con alta variabilidad.
- Sistema de calidad deficiente: sin procedimientos claros para reclamos, documentación inconsistente y áreas de control en condiciones higiénico-sanitarias inadecuadas.
¿Qué medidas tomó la ANMAT?
La ANMAT concluyó que no existen garantías de calidad ni en la materia prima ni en el producto terminado, lo que representa un riesgo para la salud pública. Ante la gravedad de la situación, el organismo de control sanitario resolvió:
- Inhibir preventivamente las actividades productivas de Laboratorios Beta S.A.
- Prohibir el uso, comercialización y distribución de los lotes afectados de Exotran en todo el país.
- Ordenar el retiro del mercado de los lotes mencionados.
- Suspender el certificado REM N° 53.080 del medicamento hasta que el laboratorio implemente acciones correctivas y preventivas validadas.